ชุด PCR แบบเรียลไทม์ของไวรัส Monkeypox
รายละเอียดสินค้า
วัตถุประสงค์การใช้งาน
ใช้สำหรับการตรวจหา Monkeypox Virus ในตัวอย่างซีรั่มหรือสารหลั่งของรอยโรคของมนุษย์ โดยใช้ระบบ PCR แบบเรียลไทม์
หลักการทดสอบ
ผลิตภัณฑ์นี้คือระบบทดสอบ PCR แบบเรียลไทม์ของ Taqman® ที่ใช้โพรบฟลูออเรสเซนต์ไพรเมอร์และโพรบเฉพาะได้รับการออกแบบสำหรับการตรวจหายีน F3L ของ Monkeypox Virusการควบคุมภายในที่กำหนดเป้าหมายไปที่ยีนอนุรักษ์โดยมนุษย์จะตรวจสอบการเก็บตัวอย่าง การจัดการตัวอย่าง และกระบวนการ PCR แบบเรียลไทม์ เพื่อหลีกเลี่ยงผลลัพธ์ที่เป็นลบลวงชุดนี้เป็นระบบพรีมิกซ์ไลโอฟิไลซ์เต็มรูปแบบ ซึ่งประกอบด้วยวัสดุที่จำเป็นสำหรับการตรวจหาไวรัส Monkeypox: เอนไซม์ขยายกรดนิวคลีอิก เอนไซม์ UDG บัฟเฟอร์ปฏิกิริยา ไพรเมอร์เฉพาะ และโพรบ
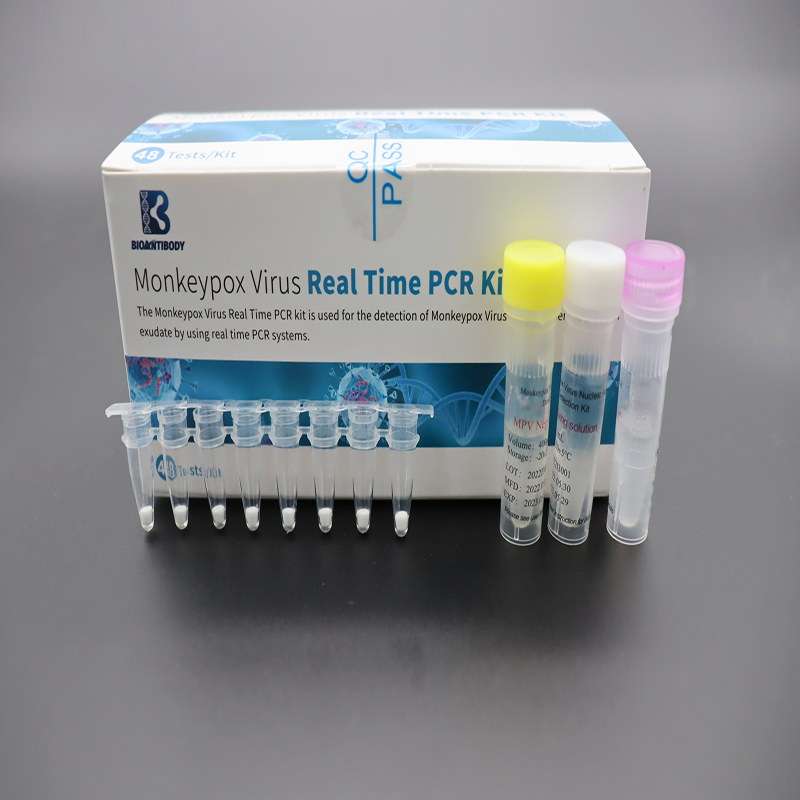
เนื้อหาหลัก
ส่วนประกอบที่ให้ไว้แสดงอยู่ในตาราง
| ส่วนประกอบ | บรรจุุภัณฑ์ | วัตถุดิบ |
| ไวรัสโรคฝีลิงพรีมิกซ์แบบไลโอฟิไลซ์ | หลอด PCR จำนวน 8 เส้น× 6 ถุง | ไพรเมอร์, โพรบ, dNTP/dUTP Mix, Mg2+, Taq DNA polymerase, เอนไซม์ UDG |
| MPV การควบคุมเชิงบวก | 400 ไมโครลิตร×1 หลอด | ลำดับดีเอ็นเอที่มียีนเป้าหมาย |
| การควบคุมเชิงลบของ MPV | 400 ไมโครลิตร×1 หลอด | ลำดับดีเอ็นเอที่มีส่วนของยีนมนุษย์ |
| สารละลายละลาย | 1 มล.×1 หลอด | โคลง |
| ใบรับรองความสอดคล้อง | 1 ชิ้น | / |
กระแสการดำเนินงาน
1. ตัวอย่างของสะสม:ควรเก็บตัวอย่างใส่หลอดปลอดเชื้อตามที่กำหนด
ด้วยข้อกำหนดทางเทคนิคมาตรฐาน
2. การเตรียมรีเอเจนต์ (พื้นที่เตรียมรีเอเจนต์)
นำส่วนประกอบของชุดอุปกรณ์ออกมา ปรับสมดุลที่อุณหภูมิห้องเพื่อใช้งานในโหมดสแตนด์บาย
3. การประมวลผลตัวอย่าง (พื้นที่การประมวลผลตัวอย่าง)
3.1 การสกัดกรดนิวคลีอิก
ขอแนะนำให้เก็บตัวอย่างของเหลวขนาด 200μL แบบควบคุมเชิงบวกและแบบลบสำหรับการสกัดกรดนิวคลีอิก ตามข้อกำหนดและขั้นตอนที่เกี่ยวข้องของชุดสกัด DNA ของไวรัส
3.2 การละลายผงไลโอฟิไลซ์และการเติมเทมเพลต
เตรียมพรีมิกซ์ Monkeypox Virus Lyophilized ตามจำนวนตัวอย่างตัวอย่างหนึ่งรายการต้องใช้หลอด PCR หนึ่งหลอดที่มีผงพรีมิกซ์ไลโอฟิไลซ์การควบคุมเชิงลบและการควบคุมเชิงบวกควรถือเป็นสองตัวอย่าง
(1) เติมสารละลายละลาย 15μL ลงในหลอด PCR แต่ละหลอดที่มีพรีมิกซ์แบบ Lyophilized จากนั้นเติมตัวอย่างที่สกัดแล้ว 5μL/ การควบคุมเชิงลบ/การควบคุมเชิงบวก ลงในหลอด PCR แต่ละหลอดตามลำดับ
(2) ปิดหลอด PCR ให้แน่น สะบัดหลอด PCR ด้วยมือจนกระทั่งผงไลโอฟิไลซ์ละลายและผสมจนหมด เก็บของเหลวไว้ที่ด้านล่างของหลอด PCR โดยการปั่นแยกด้วยความเร็วต่ำทันที
(3) หากใช้เครื่องมือ PCR แบบเรียลไทม์ทั่วไปในการตรวจจับ ให้ย้ายหลอด PCR ไปยังพื้นที่ขยายโดยตรงหากใช้ BTK-8 ในการตรวจจับ จะต้องดำเนินการต่อไปนี้: ถ่ายโอนของเหลว 10 μL จากหลอด PCR ไปยังชิปปฏิกิริยาของ BTK-8ท่อ PCR หนึ่งท่อตรงกับหนึ่งช่องบนชิปในระหว่างการดำเนินการปิเปต ตรวจสอบให้แน่ใจว่าปิเปตอยู่ในแนวตั้ง 90 องศาควรวางทิปปิเปตกั้นละอองลอยไว้ตรงกลางบ่อโดยใช้แรงปานกลาง และหยุดดันปิเปตเมื่อถึงเกียร์แรก (เพื่อหลีกเลี่ยงฟองอากาศ)หลังจากเติมหลุมแล้ว ให้นำเมมเบรนชิปปฏิกิริยาออกมาเพื่อครอบคลุมหลุมทั้งหมด จากนั้นชิปจะถูกถ่ายโอนไปยังพื้นที่ตรวจจับการขยายสัญญาณ
4. การขยาย PCR (พื้นที่การตรวจจับ)
4.1 ใส่ท่อ PCR/ชิปปฏิกิริยาลงในถังปฏิกิริยา และตั้งชื่อของแต่ละปฏิกิริยาตามลำดับที่สอดคล้องกัน
4.2 การตั้งค่าการตรวจจับเรืองแสง: (1) Monkeypox virus (FAM);(2) การควบคุมภายใน (CY5)
4.3 เรียกใช้โปรโตคอลการขี่จักรยานต่อไปนี้
โปรโตคอลของ ABI7500, Bio-Rad CFX96, SLAN-96S, QuantStudio:
| ขั้นตอน | อุณหภูมิ | เวลา | รอบ | |
| 1 | การเสียสภาพก่อนกำหนด | 95 ℃ | 2 นาที | 1 |
| 2 | การเสียสภาพ | 95 ℃ | 10 วิ | 45 |
| การหลอม การขยาย การได้มาของสารเรืองแสง | 60 ℃ | 30 วิ | ||
พิธีสารของ BTK-8:
| ขั้นตอน | อุณหภูมิ | เวลา | รอบ | |
| 1 | การเสียสภาพก่อนกำหนด | 95 ℃ | 2 นาที | 1 |
| 2 | การเสียสภาพ | 95 ℃ | 5 วิ | 45 |
| การหลอม การขยาย การได้มาของสารเรืองแสง | 60 ℃ | 14 วิ | ||
5. การวิเคราะห์ผลลัพธ์ (โปรดดูคู่มือผู้ใช้เครื่องมือ)
หลังจากปฏิกิริยา ผลลัพธ์จะถูกบันทึกโดยอัตโนมัติคลิก "วิเคราะห์" เพื่อวิเคราะห์ จากนั้นเครื่องมือจะตีความค่า Ct ของแต่ละตัวอย่างในคอลัมน์ผลลัพธ์โดยอัตโนมัติผลการควบคุมเชิงลบและบวกจะต้องเป็นไปตาม "6. การควบคุมคุณภาพ" ต่อไปนี้
6. ควบคุมคุณภาพ
6.1 การควบคุมเชิงลบ: ไม่มี Ct หรือ Ct>40 ในช่อง FAM, Ct≤40 ในช่อง CY5 พร้อมกราฟการขยายปกติ
6.2 การควบคุมเชิงบวก: Ct≤35 ในช่อง FAM พร้อมกราฟการขยายปกติ, Ct≤40 ในช่อง CY5 พร้อมกราฟการขยายปกติ
6.3 ผลลัพธ์จะถือว่าถูกต้องหากเป็นไปตามเกณฑ์ข้างต้นทั้งหมดมิฉะนั้นผลลัพธ์จะไม่ถูกต้อง
การตีความผลลัพธ์
ผลลัพธ์ต่อไปนี้เป็นไปได้:
| ค่ากะรัตของช่อง FAM | ค่า Ct ของช่อง CY5 | การตีความ | |
| 1# | ไม่มี Ct หรือ Ct > 40 | ≤40 | ไวรัส Monkeypox เป็นลบ |
| 2# | ≤40 | ผลลัพธ์ใดๆ | ไวรัส Monkeypox เป็นบวก |
| 3# | 40~45 | ≤40 | ทดสอบซ้ำ;ถ้ายังคงเป็น 40~45 ให้รายงานเป็น 1# |
| 4# | ไม่มี Ct หรือ Ct > 40 | ไม่มี Ct หรือ Ct > 40 | ไม่ถูกต้อง |
บันทึก: หากผลลัพธ์ไม่ถูกต้อง จะต้องรวบรวมตัวอย่างและทดสอบอีกครั้ง
ข้อมูลการสั่งซื้อ
| ชื่อผลิตภัณฑ์ | แมว.เลขที่ | ขนาด | ตัวอย่าง | อายุการเก็บรักษา | ทรานส์& สโตอุณหภูมิ |
| ชุด PCR แบบเรียลไทม์ของไวรัส Monkeypox | B001P-01 | การทดสอบ 48 ครั้ง/ชุด | เซรั่ม/ Lesion Exudate | 12 เดือน | -25~-15℃ |